ایزوبارها عناصری هستن که از نظر خواص شیمیایی با هم تفاوت دارن ولی ویژگی فیزیکی یکسانی دارن. پس میشه گفت که ایزوبارها اون دسته از عناصری هستن که عدد اتمی متفاوت اما عدد جرمی یکسانی دارن. در مقابل، ایزوتوپها اون دسته از عناصری هستن که عدد اتمی یکسان و اعداد جرمی متفاوتی دارن.
در ادامه این مطلب از سایت دیفرتو ویژگیهای این دو مقوله رو بیشتر توضیح میدیم. پس اونها رو مطالعه کنین تا بهتر درک کنین که تفاوت ایزوتوپ و ایزوبار چیه.
ایزوبار (Isobar) چی هستن؟
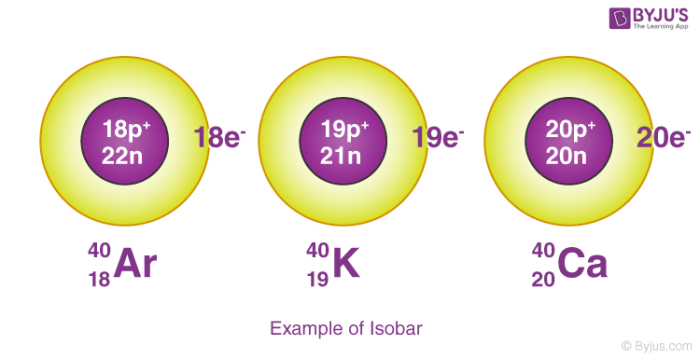
ایزوبار اتمها عناصر شیمیایی مختلفی هستن که از نظر ویژگی شیمیایی متفاوتن اما ویژگی فیزیکی یکسانی دارن. پس میشه گفت که ایزوبارها اون دسته از عناصری هستن که عدد اتمی متفاوتی دارن اما عدد جرمیشون یکسانه. خاصیت شیمیایی اونها متفاوته چون در تعداد الکترونها تفاوت وجود داره. جرم اتمی اون یکسانه اما عدد اتمی اون متفاوته. این حالت به این دلیله که تعداد اضافی نوترون، تفاوت در تعداد نوکلئونها رو جبران میکنه.
یک مثال از دو ایزوتوپ و ایزوبار آهن و نیکله که هر دو عدد جرمی یکسانی دارن که برابر با ۵۸ هست، درحالیکه عدد اتمی آهن ۲۶ و عدد اتمی نیکل ۲۸ هست.
- مقاله مرتبط: تفاوت اتم با یون
ایزوتوپ (Isotope) چی هستن؟
اجازه بدین دو چیز رو مثال بزنیم که رنگ یکسان و ظاهر فیزیکی یکسانی دارن، به طوری که شما نمیتونین بین این دو تمایز قائل بشین. اما وقتی وزن این دو چیز رو اندازهگیری میکنی، متوجه میشین که اونها متفاوت هستن. با این مثال میتونین مفاهیم ایزوتوپ رو به هم مرتبط کنین.
همونطور که همه ما میدونیم اتمها از الکترون، پروتون و نوترون تشکیل شدن. هسته از پروتونها و نوترونها تشکیل شده و الکترونها به دور هسته میچرخن. جرم اتمی مجموع تعداد پروتون و نوترون و عدد اتمی برابر با تعداد پروتونهاس. توی یک عنصر، تعداد پروتونها همیشه یکسان هستن، اما تعداد نوترونها مدام در حال تغییره.
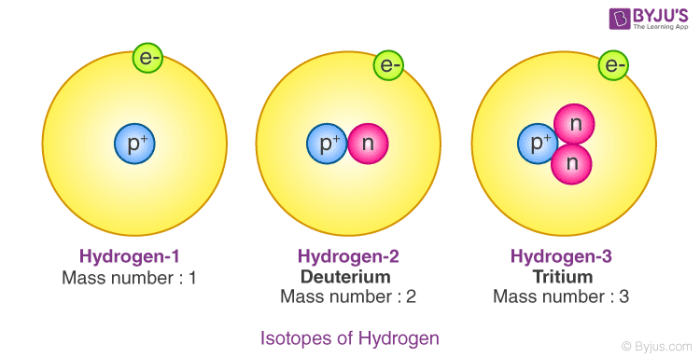
ایزوتوپها اتمهایی هستن که تعداد نوترونهای اونها متفاوتن و تعداد پروتونهای یکسانی دارن. از تعریف فوق برای جرم اتمی و عدد اتمی، میشه نتیجه گرفت که ایزوتوپها اون دسته از عناصری هستن که عدد اتمی یکسان و اعداد جرمی متفاوتی دارن. در مورد ایزوتوپهای هیدروژن: سه ایزوتوپ هیدروژن وجود داره که شامل پروتیوم، دوتریوم و تریتیوم میشه.
هر سه اونها تعداد پروتونهای یکسانی دارن، اما تعداد نوترونها متفاوته. توی پروتیوم تعداد نوترونها صفر، توی دوتریوم یک و توی تریتیوم تعداد نوترونها دوتاس.
- مقاله مرتبط: تفاوت یون و ایزوتوپ
فرق بین ایزوتوپ و ایزوبار چیه؟
جدول زیر چند تفاوت بین ایزوتوپها و ایزوبارها رو نشون میده.
| ایزوبارها | ایزوتوپها |
| عناصر شیمیایی که جرم یکسانی دارن | ساختار اتمی متفاوت یک عنصر |
| جرم اتمی برابره | جرم اتمی متفاوته |
| اغلب خواص فیزیکی مشابه دارن | معمولاً خواص فیزیکی متفاوت دارن |
| اعداد اتمی متفاوته | اعداد اتمی یکسان هستن |
| عناصر شیمیایی متفاوتن | عناصر شیمیایی یکسان با اعداد جرمی متفاوت |
جمعبندی
در آخر باید بگیم که ایزوتوپها اتمهایی هستن که تعداد پروتون مساوی دارن ولی تعداد نوترون و پروتون اونها متفاوته. چند مثال از ایزوتوپهای پایدار که میتونیم بگیم شامل وانادیم، کربن، کلسیم، پتاسیم هستن. ایزوتوپهای ناپایدار پرتوهایی رو از خودشون ساطع میکنن که شامل پرتوهای آلفا، بتا و گاما میشه.
ایزوبارها اتمهایی هستن که عدد جرمی یکسانی دارن اما تعداد پروتونهای اونها متفاوتی هستن. چند نمونه از ایزوبارها شامل 40S، 40Ar، 40Ca. 40Cl و 40K میشه.
به نظر شما فرق ایزوتوپ و ایزوبار که در این مقاله توضیح داده شد، درست بوده؟ اگر شما اطلاعات بیشتری از تفاوت ایزوتوپ و ایزوبار میدونید یا فکر میکنید تعریف دقیقتری وجود داره، حتما در بخش نظرات، برای ما ارسال کنید تا مقاله رو اصلاح و تکمیل کنیم.
منبع: byjus.com

